
les doy la bienvenida a mi blog de las reacciones endo exo termicas deleitense con mi trabajo ;)
Se denomina reacción exotérmica a cualquier reacción química que desprende calor, es decir con una variación negativa de entalpía.Se da principalmente en las reacciones de oxidación. Cuando ésta es intensa puede dar lugar al fuego. Cuando reaccionan entre sí dos átomos de hidrógeno para formar una molécula, el proceso es exotérmico.
- H· + H· → H:H
- ΔH = -104 kcal/mol
Son cambios exotérmicos el paso de gas a líquido (condensación) y de líquido a sólido (solidificación).
La reacción contraria se denomina endotérmica.
Un ejemplo de reacción exotérmica es la combustión.
una reaccion exotermica es la que al formarse desprende energia(calor).
El prefijo exo significa “hacia fuera”. Por lo tanto entendemos que las reaccionesexotérmicas son aquellas que liberan energía en forma de calor. El esquema general de una reacción exotérmica puede ser escrito de la manera siguiente, donde A, B, C y D representan sustancias genéricas.
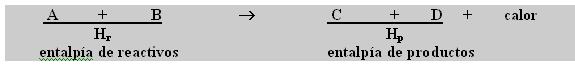
A partir de la Ley de la Conservación de Energía, podemos afirmar que “La energía total de los reactivos es igual a la energía total de los productos”.
En otras palabras, toda la energía que entró en el primer miembro de la ecuación química, debe salir íntegramente en el segundo miembro de la ecuación. De donde obtenemos la siguiente conclusión: si una reacción es exotérmica, entonces la entalpía de los reactivos (Hr ) es mayor que la entalpía de los productos(Hp ), pues una parte de la energía que estaba contenida en los reactivos fue liberada para el medio ambiente en forma de calor y apenas otra parte de esa energía quedó contenida en los productos. Entonces en una reacción exotérmica: Hr > Hp
No es posible determinar directamente la entalpía de cada sustancia participante de una reacción, pero podemos determinar experimentalmente la variación de entalpía ΔH, que ocurre cuando una reacción química es realizada.

Como en la reacción exotérmica Hr > Hp , entonces en este tipo de reacción el valor de ΔH será siempre negativo. Siendo que la reacción exotérmica: ΔH > 0.
Observa que no existe energía negativa; un sistema contiene energía. El signo negativo de DH quiere decir apenas que la energía fue liberada.





REACCIONES ENDOTERMICAS .
En las reacciones químicas endotérmicas se absorbe calor, DH es positivo y significa que la energía de los productos es mayor que la energía de los reactivos, por ejemplo en la fotosíntesis.
REACCIONES ENDOTÉRMICAS
El prefijo endo significa “hacia adentro”. Por lo tanto se entiende que las reacciones endotérmicas son aquellas que absorben energía en forma de calor. El esquema general de una reacción endotérmica puede ser escrito de la siguiente manera, donde A, B, C y D representan sustancias genéricas.

Una vez que la energía total se conserva del primer para el segundo miembro de cualquier reacción química, podemos afirmar que: si una reacción es endotérmica, la entalpía de los productos Hp es mayor que la entalpía de los reactivos Hr , pues una determinada cantidad de energía fue absorbida por los reactivos en forma de calor, durante la reacción, quedando contenida en los productos. Siendo que en la reacción endotérmica: Hp> Hr.
Y siendo DH = Hp — Hr , entonces en la reacción endotérmica el valor de ΔH será siempre positivo. Siendo que en la reacción endotérmica: ΔH > 0.
más estabilidad = menos energía = menor ΔH = reacción más espontánea
Tal que podemos utilizar el ejemplo: Agregándose los gases F2, Cl2 e Br2 a un recipiente conteniendo gas hidrógeno, puede preverse cual será la reacción que ocurrirá primero a través del valor de ΔH de cada una.

Reacciones endotérmicas: son aquellas reacciones que absorben calor, lo que significa que la energía de las moléculas de los productos (EP) es mayor que la energía de las moléculas de los reaccionantes (ER).
La reacción para obtener N2O es un proceso endotérmico que requiere calor para unir al nitrógeno y el oxígeno, la cantidad de calor se representa en Kcal.
2N2(g) + O2(g) + 39 Kcal 2N2O(g)
2N2O(g)
2N2(g) + O2(g) + 39 Kcal




Reacciones exotérmicas y reacciones endotérmicas:
Durante las reacciones químicas puede producirse absorción o liberación de energía. Esto indica que tanto los reaccionantes como los productos contienen calor que es característico de su masa. El contenido de calor es una medida de la energía que está acumulada por una sustancia durante su formación.
Durante las reacciones químicas puede producirse absorción o liberación de energía. Esto indica que tanto los reaccionantes como los productos contienen calor que es característico de su masa. El contenido de calor es una medida de la energía que está acumulada por una sustancia durante su formación.

La energía se conserva durante las reacciones químicas. En una reacción pueden considerarse dos fases diferenciadas: en primer lugar, los enlaces químicos de los reactivos se rompen, y luego se reordenan constituyendo nuevos enlaces. En esta operación se requiere cierta cantidad de energía, que será liberada si el enlace roto vuelve a formarse. Los enlaces químicos con alta energía se conocen como enlaces `fuertes', pues precisan un esfuerzo mayor para romperse. Si en el producto se forman enlaces más fuertes que los que se rompen en el reactivo, se libera energía en forma de calor, constituyendo una reacción exotérmica. En caso contrario, la energía es absorbida y la reacción se denomina endotérmica. Debido a que los enlaces fuertes se crean con más facilidad que los débiles, son más frecuentes las reacciones exotérmicas espontáneas; un ejemplo de ello es la combustión de los compuestos del carbono en el aire para producir CO2 y H2O, que tienen enlaces fuertes. Pero también se producen reacciones endotérmicas espontáneas, como la disolución de sal en agua.
Las reacciones endotérmicas suelen estar asociadas a la disociación de las moléculas. Esto último puede medirse por el incremento de la entropía del sistema. El efecto neto de la tendencia a formar enlaces fuertes y la tendencia de las moléculas e iones a disociarse se puede medir por el cambio en la energía libre del sistema. Todo cambio espontáneo a temperatura y presión constantes implica un incremento de la energía libre, acompañado de un aumento de la fuerza del enlace.
marco teorico : las reacciones endotermicas y exotermicas se pueden definir facilmente como
reaccion endotermica :El prefijo endo significa “hacia adentro”. Por lo tanto se entiende que las reacciones endotérmicas son aquellas que absorben energía en forma de calor.
reaccion exotermica :El prefijo exo significa “hacia fuera”. Por lo tanto entendemos que las reaccionesexotérmicas son aquellas que liberan energía en forma de calor.
una palabra clave puede ser entalpia
entalpia :
| Entalpía: es el contenido calórico de una sustancia y se representa con la letra H. La variación de entalpía en un sistema químico , de las reacciones endotermicas puede ser un incendio , un horno , la tetera porque son ejempos que absorven energia . y las reacciones exotermicas como ejemplo se puede dar encender un fosforo la estufa una fogata . reaccion quimica : | |
| Una reacción química o cambio químico o fenómeno químico es todo proceso químico en el cual una o más sustancias (llamadasreactivos), por efecto de un factor energético, se transforman en otras sustancias llamadas productos. Esas sustancias pueden serelementos o compuestos |
Reacción de oxidación: Es la capacidad que tiene una sustancia a ceder sus electrones frente a otra que actúa como agente oxidante. El agente oxidante se reduce captando los electrones del dador, el dador adquiere la forma oxidada. Ambas sustancias actúan como una pila galvánica ya que se establece una corriente de electrones entre ambas semipilas.
webgrafia: